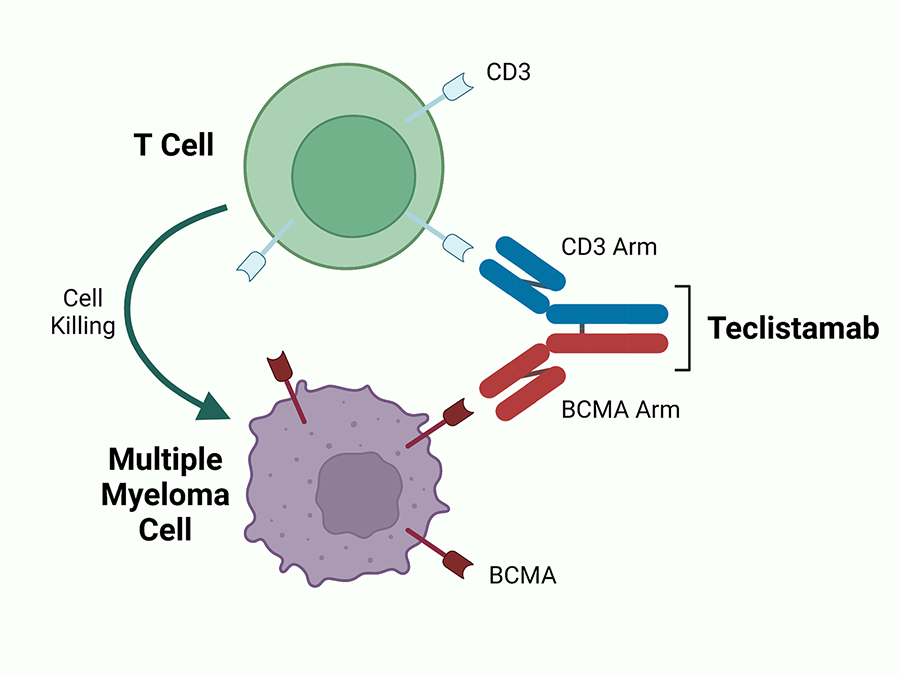
Teclistamab er et såkaldt bispecifikt antistof. Det betyder, at det forbinder kræftcellen med kroppens egne T-celler. T-cellerne tilintetgør derefter kræftcellen.
Behandlingen er godkendt til patienter der har fået mindst tre forudgående behandlingslinjer og har tilbagefald.
Medicinrådets godkendelse er betinget af at man opsamler data på bivirkninger ved brugen af behandlingen, og man vil efter et til to år genvurdere godkendelsen.
Teclistamab har i forsøgsprotokoller vist sig at have effekt på mere end to tredjedele af de patienter der indgik. Og ca. 25% opnåede at sygdommen ikke kunne måles. Patienterne i forsøget havde i gennemsnit modtaget frem forudgående behandlingslinjer og enten ikke oplevet effekt eller havde fået tilbagefald.
Medicinrådets anbefaling vedr. teclistamab til knoglemarvskræft
Medicinrådet anbefaler teclistamab til voksne patienter med recidiverende og refraktær knoglemarvskræft (myelomatose), som har fået mindst tre tidligere behandlinger, herunder et immunmodulerende lægemiddel, en proteasomhæmmer samt et anti-CD38-antistof, og som har haft sygdomsprogression under seneste behandling. Anbefalingen gælder patienter, som er i god almen tilstand (performancestatus 0-1).
Medicinrådet vurderer, at behandling med teclistamab udskyder tiden til sygdoms-progression og øger patienternes overlevelse sammenlignet med nuværende standardbehandling, som er pomalidomid – eller carfilzomib-holdig behandling. Det er meget usikkert, hvor stor effekten er, da teclistamab kun er undersøgt i et enkeltarmet ukontrolleret studie, dvs. uden direkte sammenligning med andre behandlingsmuligheder. Teclistamab er forbundet med risiko for alvorlige bivirkninger.
Behandling med teclistamab er dyrere end nuværende standardbehandling. Samlet set vurderer Medicinrådet dog, at omkostningerne er rimelige i forhold til effekten for denne patientgruppe.
Grundet risiko for alvorlige bivirkninger og usikkerhed om effekten forudsætter Medicinrådets anbefaling, at der i klinikken systematisk indsamles effekt- og bivirkningsdata for patienter, som behandles med teclistamab.
Medicinrådet vil efter ét og to år på baggrund af indleveret data tage stilling til, om anbefalingen fortsat skal gælde.