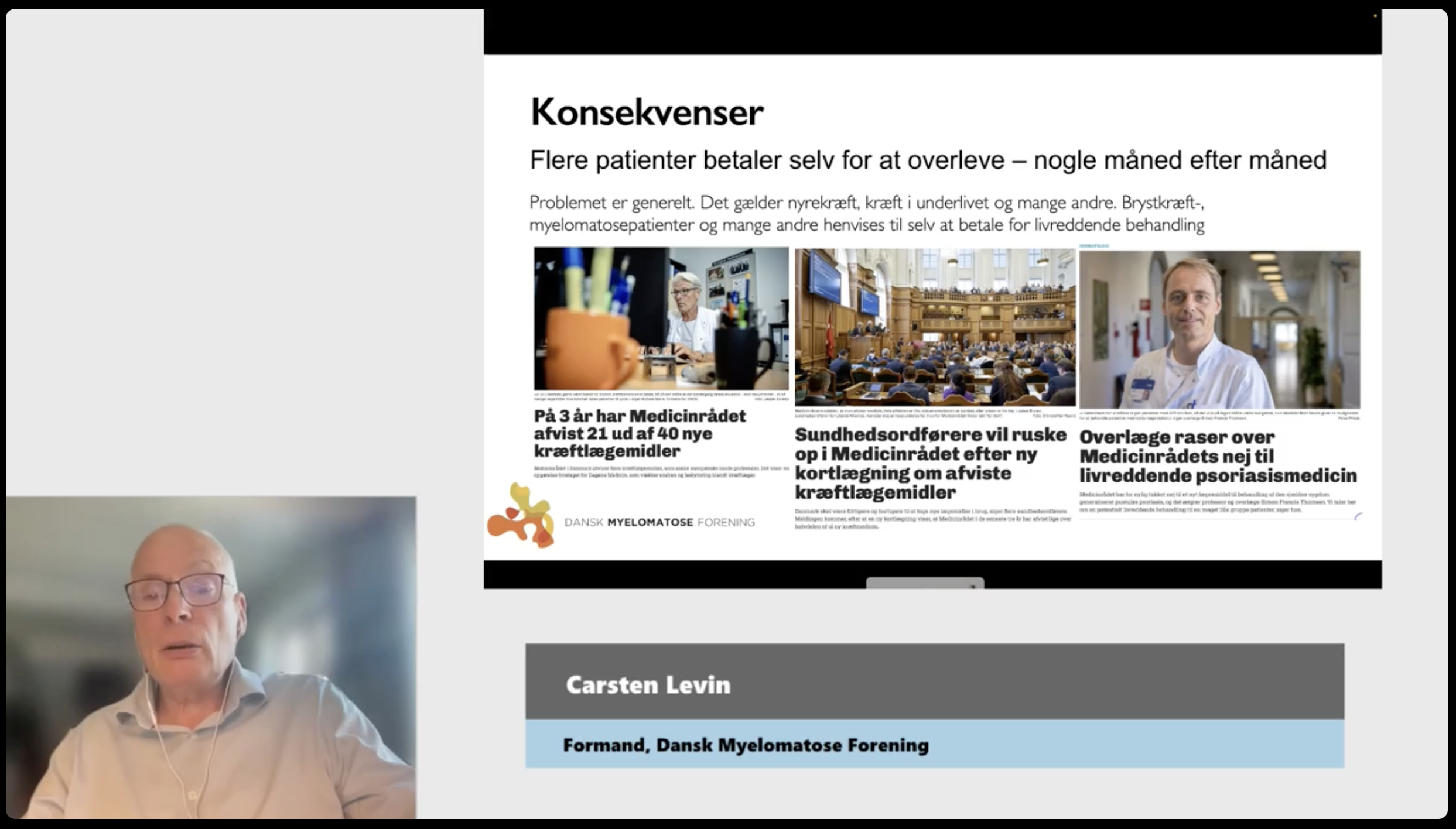
Den 25. marts ansøgte virksomheden bag CAR-T-cellebehandlingen cilta-cel, Johnson & Johnson, om, at Medicinrådet skal revurdere sin afvisning af denne behandling. I sidste uge kom svaret fra Medicinrådet endelig: Man har vedtaget at genoptage sagen. Dansk Myelomatose Forening ser meget positivt på denne beslutning, og håber, at det denne gang fører til en anbefaling af CAR-T-celler som standardbehandling af knoglemarvskræft.
Pårørendeseminar 2024
I år afholdes pårørendeseminaret både i Aarhus og i København
Arrangementerne for de pårørende gennemføres af Myelomatoseforenigen i samarbejde med Kræftens Bekæmpelses lokalforeninger og andre patientforeninger.
Din næste samtale med sundhedsvæsenet kan ændre dit liv
Din næste samtale med sundhedsvæsenet kan ændre dit liv – tag ordet!
Dansk Selskab for PatientSikkerhed har lavet en meget fin vejledning i den svære kunst: At forberede, gennemføre og at samle op efter konsultationen med læger og andet sundhedspersonale.